Resultado Proyecto
Sarcoptes scabiei: caracterización de la respuesta inmune y valoración del potencial vacunal de distintos preparados antigénicos en conejo
Referencia: RTA2011-00087-00-00. Organismo financiador: Ministerio de Ciencia e Innovación Instituto Nacional de Investigación y Tecnología Agraria y Alimentaria Cofinanciado por el Fondo Europeo de Desarrollo Regional. Importe: 60.540 €. Duración: 2011-2015.
 |
 |
 |
Equipo investigador
Rosa Casais Goyos. SERIDA
José Miguel Prieto Martín. SERIDA
Ana del Cerro Arrieta. SERIDA
Angel Venteo Moreno. Inmunología y Genética Aplicada, S.A.
Isabel García Soto. Inmunología y Genética Aplicada, S.A.
Equipo técnico
Paloma Solano Sobrado. SERIDA
Resultados y conclusiones
El presente proyecto abordó el estudio de los mecanismos de respuesta inmune, la identificación de antígenos inmunodominantes de S. scabiei, y la evaluación del potencial vacunal de dichos antígenos en el modelo animal conejo/S. scabiei var. cuniculi, con el objeto de desarrollar una vacuna eficaz para llevar a cabo el control de la sarna sarcóptica.
1) Monitorización clínica y caracterización de la respuesta inmune primaria y secundaria en conejos infestados experimentalmente con el ácaro S. scabiei, tratados con ivermectina, curados, y reinfectados con la misma variedad de S. scabiei.
La infestación se realizó por dos métodos: contacto directo con un conejo infestado (n=10, 5 hembras y 5 machos) y colocación de una venda portadora de 1800 ácaros en cada pata trasera (n=10, 5 hembras y 5 machos). El modelo animal S. scabiei/conejo de infestación por contacto sirve para comprender mejor la reacción del hospedador durante una infección natural, mientras que el modelo mediante venda permite controlar la dosis específica que recibe cada individuo y el punto de inoculación, este último parece el modelo más adecuado para realizar ensayos de vacunación.
El progreso de la enfermedad fue marcadamente más virulento en los animales infestados por contacto directo, indicando que la dosis efectiva de ácaros que logran prósperar e infestar cada conejo por este método es más alta. La infestación por contacto indujo protección parcial (se observó retraso en la aparición de las primeras lesiones y una pequeña disminución en la extensión de las mismas), los animales produjeron niveles altos de IgG no-protectoras tras la re-exposición mostrando signos clínicos severos. Sin embargo, los animales infestados mediante el método de la colocación de una venda desarrollaron títulos más bajos de IgGs pero mostraron niveles altos de resistencia frente a la reinfección (animales sin lesiones o con puntuaciones muy bajas). Esto podría deberse a la inducción de una fuerte respuesta inmune celular local en el punto de inoculación de los ácaros que diese lugar a una dosis infectiva más baja. El análisis estadístico de los datos mostró que el sexo, la ruta de infección y la exposición previa son factores que determinan la capacidad de los conejos para desarrollar inmunidad protectora frente a esta enfermedad.
2) Ensayo del potencial vacunal de distintos preparados antigénicos.
La vacunación es una alternativa atractiva frente al uso de acaricidas para llevar a cabo el control de parásitos. Sin embargo, hasta el momento no se han desarrollado vacunas efectivas frente a la sarna sarcóptica. El propósito último de este estudio ha sido el desarrollo de una vacuna frente a la sarna sarcóptica.
Se han seleccionado y caracterizado dos antígenos inmunodominantes (Ssλ15 y Ssλ20) de sarcoptes mediante el escrutinio de una genoteca de cDNA de S. scabiei var. Hominis. Estos nuevos antígenos no presentaban homología con ninguna de las proteínas depositadas en las bases de datos. En la figura 1 se muestra la inmuno-localización de estos antígenos en los tejidos del ácaro en cortes histológicos de piel de un rebeco infestado.
La inmunización de conejos (n=8) con una mezcla de los dos antígenos seleccionados induce una respuesta inmune humoral (IgG e IgEs) elevada así como niveles altos de citoquinas pro-inflamatorias (IL-1 y TNFα), sin embargo, confiere protección parcial frente al desafío con 2500 ácaros de S. scabiei. Los animales vacunados presentan lesiones significativamente más extensas (p=0,05) (Figura 2) pero densidades de ácaros más bajas que las observadas en el grupo control. Estos resultados parecen indicar que las lesiones observadas no se deben únicamente a los ácaros sino también a una respuesta inmunológica exacerbada frente al inóculo de S. scabiei, de ahí los altos niveles de citoquinas pro-inflamatorias detectadas tras el desafío.
En conclusión, los antígenos seleccionados producidos como antígenos recombinantes no tienen eficacia clínica protectora frente a la infestación con S. scabiei aunque la inmunización logra reducir la densidad de ácaros en las lesiones. Por ello, es necesario estudiar sistemas de producción de antígenos, adyuvantes, estrategias de inmunización y combinaciones de antígenos alternativos para lograr estimular respuestas inmunes protectoras frente a la infestación por S. scabiei.
Figura 1. Inmunolocalización de los antígenos Ssλ15 y Ssλ20 en secciones de piel de un rebeco infestado con S. scabiei. La detección se realizó mediante la técnica peroxidasa anti-peroxidasa utilizando un suero policlonal de conejo anti- Ssλ15 (A y B, Barra 50 µm), un suero policlonanal anti-Ssλ20 (C, Barra 20 µm), y un suero pre-inmune de conejo (D, Barra 20 µm). A, parte anterior del ácaro; P, parte posterior del ácaro; IT el tegumento interno de la epidermis; S, bloques del estómago; M, boca; L, patas; M, boca.
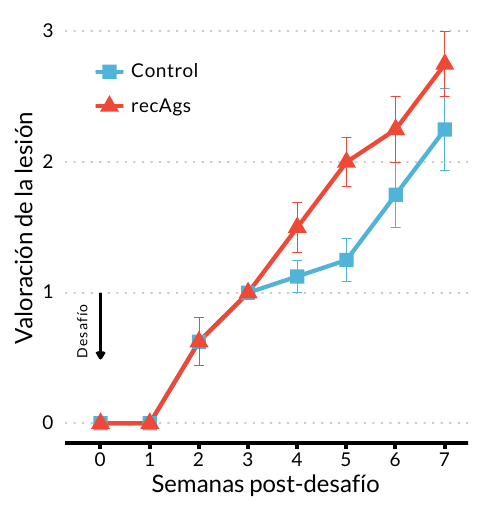
Figura 2. Evolución de las lesiones en conejos New Zealand White inmunizados y desafiados con S. scabiei. recAgs se refiere al grupo de animales inmunizado con una mezcla de los antígenos Ssλ15 y Ssλ20 y Quil A, y Control se refiere al grupo inmunizado con PBS y Quil A. Las lesiones fueron valoradas en un rango de 0 a 4 en base a la extensión de las mismas (por ejemplo se asignó 0 cuando no se observaban lesiones y 4 cuando las lesiones tenían una extensión >31cm2).