Resultado Proyecto
Sistemática basada en la tecnología macro y micro NIRS para el control de conformidad en la gestión e inspección de materias primas y piensos para su transferencia a equipos “on site”
Referencia: RTA2008-00113-C02-01. Organismo financiador: Instituto Nacional de Investigación y Tecnología Agraria y Alimentaria. Importe: 107.400 €. Duración: 2008-2011.
Equipo investigador
Begoña de la Roza Delgado. SERIDA
Adela Martínez Fernández. SERIDA
Mª Amelia González Arrojo. SERIDA
Ana Soldado Cabezuelo. SERIDA
Mª del Valle Fernández Ibáñez. SERIDA
José R. Quevedo Pérez. Universidad de Oviedo
Ana Garrido Varo. Universidad de Córdoba
José E. Guerrero Ginel. Universidad de Córdoba
Pablo Lara Vélez. Universidad de Córdoba
Dolores Pérez Marín. Universidad de Córdoba
Augusto G. Cabrera. Universidad de Córdoba
Entidades Colaboradoras
Asturiana de Servicios Agropecuarios S.L.
Centro Intercooperativo del Campo de Asturias.
Seguridad Alimentaria del Noroeste S.L.
Cooperativa Os Irmandiños
SAPROGAL
Escuela Técnica Superior de Ingenieros Agrónomos y de Montes de la Universidad de Córdoba (UCO)
Universidad de A Coruña
Justificación
Con este proyecto se persigue poner a punto una sistemática de inspección, control y gestión de materias primas y piensos basado en instrumentos NIRS portátiles de bajo coste, con el objeto de eliminar los peligros asociados al uso de dichas materias primas antes de que éstos den lugar a problemas de salud, tanto para los humanos como para los animales, o provoquen una disminución de la producción y/o de los beneficios de ganaderos y fabricantes de piensos compuestos. Para ello es necesario:
* Establecer las especificaciones más relevantes en el control de riesgos y fraudes en materias primas.
* Optimizar las librerías espectrales y modelos quimiométricos NIRS (macro y micro) el para control de riesgos y fraudes de alimentos animales.
* Desarrollar y validar un prototipo de instrumento NIR portátil, de bajo coste, para el análisis “on-site” de alimentos animales en centros de acopio, distribución y procesamiento.
* Desarrollar programas computerizados para la captura de datos espectrales, protocolos de comunicación y actuación para el control de calidad y conformidad de alimentos para animales.
* Identificar y establecer rangos de parámetros relevantes (físicos, químicos, características tecnológicas y sustancias indeseables) en materias primas y piensos para uso en alimentación animal, de acuerdo con las regulaciones normativas y las demandas de mercado.
* Armonizar técnicas analíticas para cualificar y cuantificar los parámetros relevantes en el control de riesgos y fraudes en materias primas.
* Evaluar sistemas de medida macro-NIRS para garantizar el control de micotoxinas como sustancias indeseables, de acuerdo con los niveles establecidos y recomendados por la UE para Aflatoxina B1, Ocratoxina, Zearalenona, DON y Fumonisina B1 y B2.
* Optimizar la selección de patrones y tamaño de las bibliotecas espectrales macro y micro NIRS para la detección y cuantificación de los atributos relevantes en el control de riesgos y fraudes de alimentos animales. Desarrollo y evaluación de modelos.
Resultados y conclusiones
Evaluación del proceso de crecimiento de micotoxinas en materias primas: Detección mediante Espectroscopía en el Infrarrojo Cercano
Se ha realizado un seguimiento de la formación de micotoxinas en materias primas, evaluando su crecimiento en diferentes condiciones experimentales de humedad (15 y 29 %) y temperatura (18 y 28 ºC), con muestreos semanales a diferentes alturas en un silo diseñado a escala piloto y durante un periodo de 60 días. La determinación de las micotoxinas se efectúo por HPLC-Masas en colaboración con la Universidad de La Coruña. Se observó que, en el trigo, la Aflatoxina B1 (AFB1) sólo fue detectada en un 5,7 % de las muestras, mientras que la contaminación por Ocratoxina (OCRA) lo fue en el 34% y la Zearalenona (ZEN) en el 37%. En la figura 1 se muestra la evolución del crecimiento de la ZEN después de 45 días de almacenamiento del trigo a diferentes alturas y en las condiciones experimentales de humedades y temperatura variables.

Figura 1.- Evolución del crecimiento de Zearalenona en Trigo. A: Zona Alta, B: Zona Media, C: Zona Baja. Humedad: H1: 15%; H2: 20%. Temperatura: T1:18ºC; T2: 28ºC.
Teniendo en cuenta los resultados obtenidos, hay que resaltar que ha sido posible llevar a cabo el desarrollo de modelos cuantitativos NIRS para la detección OCRA y ZEN en trigo de grano entero, con los datos espectrales recogidos en cuatro instrumentos con diferentes ópticas, rangos espectrales y presentación de la muestra. Para la determinación de estos parámetros de contaminación fúngica, el tamaño de la ventana para recoger los espectros es tan crítico como el rango de longitudes de onda de medida del equipo. Se han obtenido coeficientes de determinación de la calibración entre 0,72 y 0,96 para la ZEN y entre 0,78 y 0,44 para la OCRA. En ambos casos, los estadísticos más bajos se obtuvieron cuando se utilizó el equipo portátil Phazir, lo que es una consecuencia de su menor rango espectral (1600- 2400 nm) y más reducida ventana (4 mm de diámetro).
Evaluación de metodologías NIRS para la transferencia espectral entre equipos portátiles on-site
Se seleccionaron 25 piensos compuestos con diferentes modos de presentación (harina, pellets pequeños, pellets grandes, etc.), procedentes del Banco de Muestras de la Universidad de Córdoba (UCO), perfectamente caracterizados en cuanto a procedencia, especie destinataria y propiedades espectrales. Se analizaron espectralmente, en modo intacto, tanto en la UCO como en el SERIDA, en cada caso con su correspondiente instrumento portátil NIRS (PhazirTM Polychromix) de características técnicas semejantes.
Se evaluaron diferentes procedimientos de clonación basados en el desarrollo de matrices que ajustan la respuesta espectral (longitud de onda-reflectancia) de ambos equipos, haciendo uso del software WinISI II v.1.05 (Foss-Tecator-Infrasoft International, Port Matilda PA, USA 2000). Se compararon espectralmente y sin pretratamiento matemático previo los espectros de los 25 piensos recogidos en ambos equipos. En la Tabla 1 se muestran las correlaciones obtenidas para las diferentes condiciones experimentales ensayadas en función del nº de muestras considerado. En la Figura 2 se muestra los espectros de 1a muestra (E12-16474) de pienso compuesto antes y después de aplicar la matriz de estandarización que mejor correlaciona los espectros de ambos equipos Esta matriz fue computada a partir de 21 espectros seleccionados con el menor RMS (error medio cuadrado).
Tabla 1.- Estadísticos de estandarización obtenidos para la clonación de los dos equipos Phazir del SERIDA y la UCO.
|
Nº de muestras |
Pretratamiento derivada |
Nº de términos |
PLS R2 |
Correlación |
Varianza explicada |
||
|---|---|---|---|---|---|---|---|
|
|
|
|
|
Master |
Host |
Master |
Host |
|
25 |
Derivada |
10 |
0.5964 |
0.5663 |
0.3139 |
0.9362 |
0.9854 |
|
25 |
No |
10 |
0.5841 |
0.9999 |
0.9059 |
0.9850 |
1.0000 |
|
21 |
No |
10 |
0.5504 |
1.0000 |
0.8844 |
0.9899 |
1.0000 |
|
20 |
No |
10 |
0.3985 |
0.9999 |
0.8800 |
0.9847 |
1.0000 |
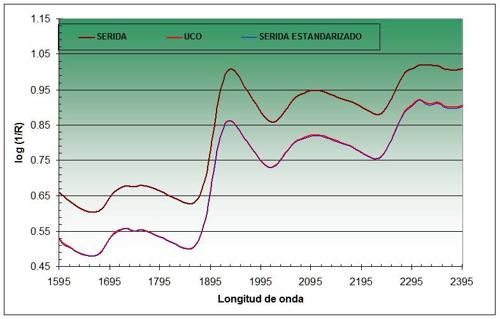
Figura 2.- Estandarización de dos equipos portátiles mediante una matriz de corrección que contiene 21 muestras de pienso compuesto.